「腸内フローラ」という言葉を耳にする機会が増えました。でも、実際にどんな仕組みで、私たちの健康にどう関わっているのでしょうか?
この記事では、薬剤師の視点から、科学的根拠に基づいて腸内フローラの基礎知識をわかりやすく解説します。
腸内フローラとは何か
腸内フローラ(intestinal flora)とは、ヒトの消化管、特に大腸に生息する膨大な数の微生物群集のことです。細菌・古細菌・真菌・ウイルスなど多種多様な微生物が含まれますが、主体は細菌です。
日本人の腸内には約1,000種・約38〜39兆個の細菌が生息しており、その総重量は約0.2 kgに達するとされています(Sender R, et al. Cell. 2016;164(3):337-340.)。
「フローラ(flora)」とは本来「植物相」を意味するラテン語で、腸内細菌が花畑のように群生している様子に由来します。近年は「腸内マイクロバイオーム(gut microbiome)」と呼ばれることも増えています。
腸内細菌の主な種類
腸内細菌は大きく3つのグループに分類されます。
善玉菌(有益菌)
代表菌:ビフィズス菌、乳酸桿菌(Lactobacillus属)
特徴:乳酸・酢酸を産生し腸内を弱酸性に保つ。病原菌の増殖を抑制する。
悪玉菌(有害菌)
代表菌:ウェルシュ菌(Clostridium perfringens)、病原性大腸菌
特徴:タンパク質を腐敗させ、アンモニアや有害物質を産生する可能性がある。
日和見菌
代表菌:バクテロイデス属、Streptococcus属の一部
特徴:腸内環境が乱れると有害な方向に働くことがある。腸内細菌の大部分を占める。
健康な状態では、善玉菌:悪玉菌:日和見菌の比率が概ね2:1:7程度に保たれているとされています(光岡知足. 腸内フローラと健康. 岩波書店, 1998年)。
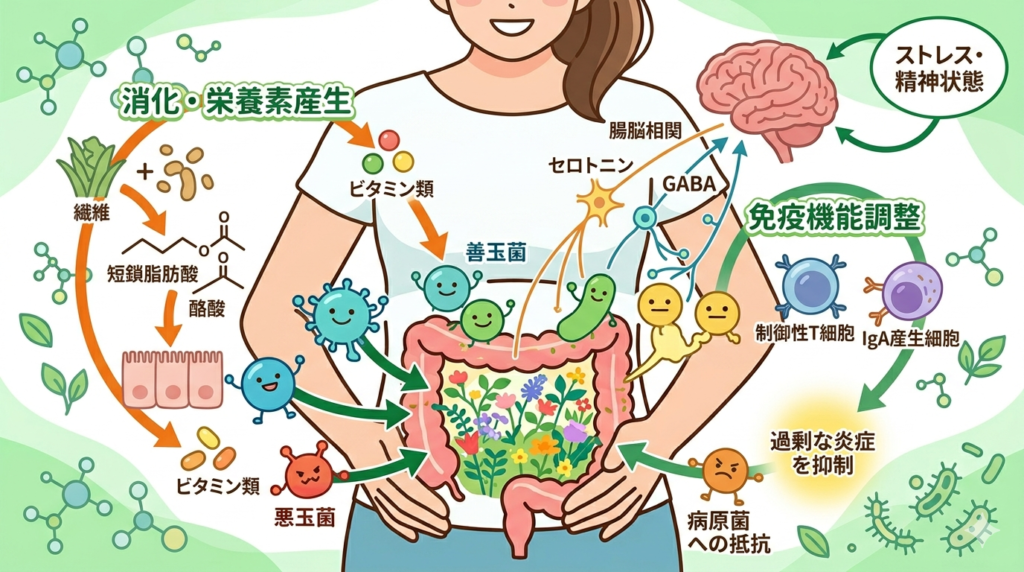
腸内フローラの主な働き
① 消化・栄養素の産生
腸内細菌は食物繊維を発酵・分解し、短鎖脂肪酸(SCFA:酢酸・プロピオン酸・酪酸)を産生します。酪酸は大腸上皮細胞の主要なエネルギー源であり、腸管バリア機能の維持に重要です。ビタミンK₂やビタミンB群(葉酸・ビオチンなど)の一部も腸内細菌が産生します(Koh A, et al. Cell. 2016;165(6):1332-1345.)。
② 免疫機能の調整
腸は体内最大の免疫器官であり、免疫細胞の約70%が集中するとされています。腸内細菌は制御性T細胞・IgA産生細胞などの分化・成熟を促し、過剰な炎症反応を抑制します。無菌マウスを用いた実験では、腸内細菌が存在しない場合に免疫機能が著しく低下することが確認されています(Hooper LV, et al. Science. 2012;336(6086):1268-1273.)。
③ 病原菌への抵抗(コロニー抵抗性)
定着している腸内細菌が栄養素や生息場所を占有することで、外来の病原菌が定着しにくい環境を作ります。これをコロニー抵抗性(colonization resistance)と呼びます(Buffie CG, Pamer EG. Nat Rev Immunol. 2013;13(11):790-801.)。
④腸脳相関(Gut-Brain Axis)
腸内細菌はセロトニンやGABAなどの神経伝達物質の産生に関与し、迷走神経を介して脳機能に影響を与えることが示されています(Cryan JF, et al. Physiol Rev. 2019;99(4):1877-2013.)。
ただし、ヒトにおける因果関係の証明はまだ研究段階であり、臨床応用には至っていない部分も多いです。
腸内フローラが乱れる原因(ディスバイオーシス)
腸内細菌のバランスが崩れた状態をディスバイオーシス(dysbiosis)と呼びます。主な原因として以下が報告されています。
抗菌薬の使用:広域抗菌薬は有益な腸内細菌も減少させ、Clostridioides difficile感染症などのリスクがあります。
食生活の偏り:食物繊維の摂取不足、高脂肪・高糖質食は腸内細菌の多様性を低下させます(Sonnenburg JL, Bäckhed F. Nature. 2016;535(7610):56-64.)。
ストレス:心理的ストレスは腸管運動や粘液分泌に影響し、腸内細菌叢を変化させます。
加齢:加齢に伴いビフィズス菌が減少し、腸内細菌の多様性が低下する傾向があります。
睡眠不足・不規則な生活リズム:概日リズムの乱れが腸内フローラのリズムにも影響することが示されています。
腸内フローラを整えるために
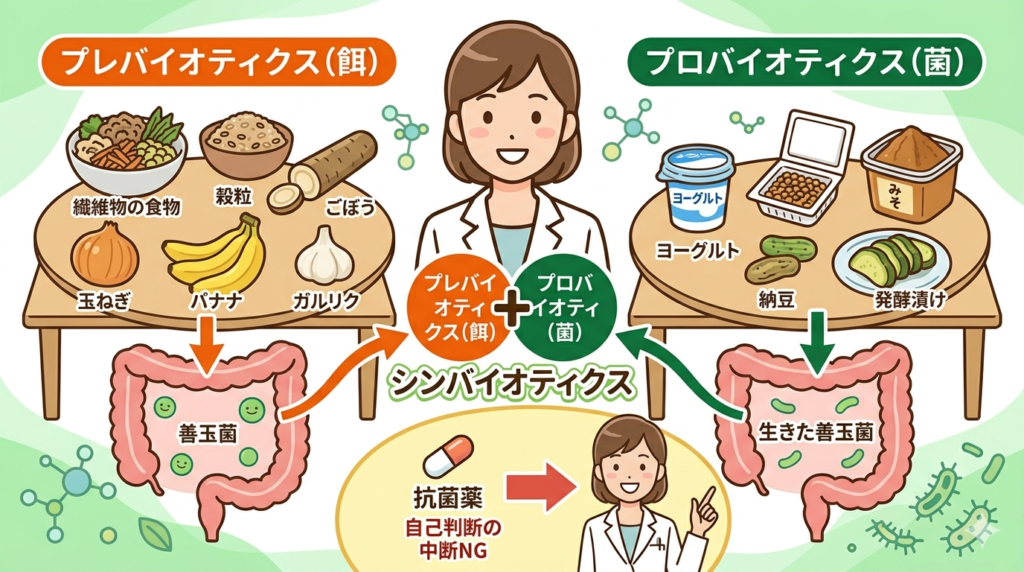
食物繊維・プレバイオティクスの摂取
食物繊維(特に水溶性食物繊維)は腸内細菌の餌となり、有益菌の増殖を促します。これをプレバイオティクスと呼びます。日本人の食物繊維摂取目標量は、成人男性で1日21g以上、成人女性で18g以上とされています(厚生労働省. 日本人の食事摂取基準2020年版)。
プレバイオティクスを多く含む食品:玉ねぎ・ごぼう・大麦・大豆・バナナ・にんにくなど。
プロバイオティクスの摂取
プロバイオティクスとは「適切な量を摂取した場合に宿主に健康上の利益をもたらす生きた微生物」と定義されています(Hill C, et al. Nat Rev Gastroenterol Hepatol. 2014;11(8):506-514.)。ヨーグルト・乳酸菌飲料・納豆・みそ・ぬか漬けなどが代表的です。
ただし、効果は菌株・用量・対象によって異なり、すべての人に同じ効果が期待できるわけではありません。特定の疾患への使用は医師・薬剤師にご相談ください。
プレバイオティクスとプロバイオティクスを同時に摂取することは相乗効果を生みます。これをシンバイオティクスといいます。
我が家の朝食はグラノーラ+ヨーグルト+はちみつ(+冷凍フルーツ)を1つのパターンとして取り入れていますが、シンバイオティクスを実践できるので重宝しています。
子供達から納豆巻きをリクエストされることもありますが、これも割と手軽に出来るシンバイオティクスだと感じます。
抗菌薬の適正使用
薬剤師として特に強調したいのが、必要のない抗菌薬使用を避けることです。ウイルス性の風邪には抗菌薬は無効であり、腸内フローラを乱すリスクだけが生じます。処方された場合は用法・用量を必ず守り、自己判断での中断はしないでください。
腸内フローラ検査:科学的根拠と限界を正しく知る
近年、自宅で受けられる腸内フローラ検査キットが普及しています。ここでは、検査の仕組み・意義・限界について、現時点の学術的知見に基づいて解説します。
検査の仕組み:次世代シーケンサーによるDNA解析
現代の腸内フローラ検査の多くは、次世代シーケンサー(NGS:Next Generation Sequencer)を用いた16S rRNAアンプリコン解析、またはショットガンメタゲノム解析によって行われます。便中に含まれる細菌のDNAを網羅的に解読することで、培養法では検出不可能だった偏性嫌気性菌を含む多数の菌種を同定できます(Turnbaugh PJ, et al. Nature. 2006;444(7122):1027-1031.)。
この技術により、以下のような情報が得られます。
- 菌種の同定と相対的な存在量:腸内に存在する細菌の種類とその比率。
- α多様性(Alpha diversity):一個人の腸内における菌種の豊富さ・均等さの指標。Shannon指数などで表されます。
- β多様性(Beta diversity):異なる個人間の腸内細菌叢の構成の違いを示す指標。
腸内フローラ検査で「わかること」と「わからないこと」
腸内フローラ研究は急速に進展していますが、検査結果の解釈には重要な限界があります。
わかること(現時点で根拠あり)
腸内細菌の多様性の低下は、肥満・2型糖尿病・炎症性腸疾患(IBD)などと関連することが複数のコホート研究で示されています(Qin J, et al. Nature. 2012;490(7418):55-60.)。
酪酸産生菌(Faecalibacterium prausnitziiなど)の減少は、クローン病・潰瘍性大腸炎患者で報告されています(Sokol H, et al. Proc Natl Acad Sci USA. 2008;105(43):16731-16736.)。
わからないこと・注意すべき限界
因果関係の未確立:腸内細菌の変化が疾患の「原因」なのか「結果」なのかは、多くの場合まだ確定していません。現時点では「関連性(相関)」が示されているにとどまるものがほとんどです。
一時点の情報である:腸内細菌叢は食事・抗菌薬・ストレス・採便方法によって短期間で変動します。一度の検査結果が「恒久的な体質」を反映するわけではありません(Lozupone CA, et al. Nature. 2012;489(7415):220-230.)。
基準値の不確立:「健康な腸内フローラ」の普遍的な基準は現時点では確立されていません。人種・地域・年齢・食文化によって正常範囲が大きく異なります(Yatsunenko T, et al. Nature. 2012;486(7402):222-227.)。
市販キットの精度差:使用するデータベース・解析手法・採便プロトコルによって結果が異なる場合があります。現時点で市販の検査キット間での標準化は十分に進んでいません。
検査結果の正しい活用方法
限界を踏まえた上で、腸内フローラ検査は「生活習慣改善の動機づけと出発点」として活用することが現実的です。具体的には以下のような活用が考えられます。
食物繊維摂取量の見直し
酪酸産生菌の餌となる水溶性食物繊維(大麦・ごぼう・玉ねぎ等)の摂取を意識する根拠として活用する。酪酸産生菌の餌となる水溶性食物繊維(大麦・ごぼう・玉ねぎ等)の摂取を意識する根拠として活用する。酪酸産生菌の餌となる水溶性食物繊維(大麦・ごぼう・玉ねぎ等)の摂取を意識する根拠として活用する。酪酸産生菌の餌となる水溶性食物繊維(大麦・ごぼう・玉ねぎ等)の摂取を意識する根拠として活用する。
発酵食品摂取の習慣化
ヨーグルト・納豆・みそ等のプロバイオティクス食品摂取の継続的習慣化の動機とする。
定期的な測定による変化の追跡:一時点の結果に一喜一憂するのではなく、生活習慣の変化前後で比較する目的で使用する。
💊注意事項(薬剤師より)
腸内フローラ検査は医療行為ではなく、疾患の診断はできません。腹痛・血便・急激な体重減少・持続する下痢や便秘など明らかな症状がある場合は、検査キットを使用する前に必ず医療機関を受診してください。
まとめ
腸内フローラは消化・免疫・神経機能など全身の健康と深く関わる複雑な生態系です。現在も世界中で研究が進む分野であり、解明されていない部分も多くあります。しかし、バランスのよい食事・適度な運動・十分な睡眠・抗菌薬の適正使用という基本的な生活習慣が、腸内フローラを整える上で現時点で最も根拠のある方法といえます。
さいごに
免責事項:本記事は一般的な健康情報の提供を目的としており、特定の疾患の診断・治療を目的としたものではありません。症状や健康上の不安がある方は、医師・薬剤師にご相談ください。
出典・参考文献
- Sender R, et al. Revised Estimates for the Number of Human and Bacteria Cells in the Body. Cell. 2016;164(3):337-340.
- Koh A, et al. From Dietary Fiber to Host Physiology: Short-Chain Fatty Acids as Key Bacterial Metabolites. Cell. 2016;165(6):1332-1345.
- Hooper LV, et al. Interactions Between the Microbiota and the Immune System. Science. 2012;336(6086):1268-1273.
- Buffie CG, Pamer EG. Microbiota-mediated colonization resistance against intestinal pathogens. Nat Rev Immunol. 2013;13(11):790-801.
- Cryan JF, et al. The Microbiota-Gut-Brain Axis. Physiol Rev. 2019;99(4):1877-2013.
- Sonnenburg JL, Bäckhed F. Diet-induced alterations in gut microflora. Nature. 2016;535(7610):56-64.
- Hill C, et al. Expert consensus document on the scope and appropriate use of the term probiotic. Nat Rev Gastroenterol Hepatol. 2014;11(8):506-514.
- 厚生労働省. 日本人の食事摂取基準(2020年版). https://www.mhlw.go.jp/stf/newpage_08517.html
- 光岡知足. 腸内フローラと健康. 岩波書店, 1998年.
- Turnbaugh PJ, et al. An obesity-associated gut microbiome with increased capacity for energy harvest. Nature. 2006;444(7122):1027-1031.
- Qin J, et al. A metagenome-wide association study of gut microbiota in type 2 diabetes. Nature. 2012;490(7418):55-60.
- Sokol H, et al. Faecalibacterium prausnitzii is an anti-inflammatory commensal bacterium identified by gut microbiota analysis of Crohn disease patients. Proc Natl Acad Sci USA. 2008;105(43):16731-16736.
- Lozupone CA, et al. Diversity, stability and resilience of the human gut microbiota. Nature. 2012;489(7415):220-230.
- Yatsunenko T, et al. Human gut microbiome viewed across age and geography. Nature. 2012;486(7402):222-227.